
【 청년일보 】 압타바이오는 비알코올성지방간염(NASH) 치료제 ‘APX-311’의 미국 특허를 취득했다고 4일 밝혔다. 압타바이오는 지난해 ‘APX-311’로 러시아·호주·일본에서 각각 특허를 획득했다. 중국과 유럽에서도 추가 특허 확보를 위해 출원을 마친 상태다. 시장 규모가 큰 국가에서 특허를 순차대로 취득해 글로벌 시장 수요에 선제 대응한다는 게 회사 측의 방침이다. NASH는 음주력이 없음에도 불구하고 알코올성 간 장애와 비슷한 병태를 나타내는 만성 질환으로 간에 지방 축적과 염증이 발생하며, 심한 경우 간경변이나 간암으로 악화될 수 있다. NASH 환자 수는 지속적으로 증가하고 있으며 시장 규모는 2026년 약 30조원에 이를 것으로 예상되지만 전 세계적으로 아직 정식 허가받은 치료제가 없는 상황이다. ‘APX-311’는 ‘NOX저해제 발굴 플랫폼’에 기반한 NASH 치료제 파이프라인이다. 현재 임상 1상 시험을 완료한 상태며 올해 임상 2상 진입을 목표로 하고 있다. 압타바이오는 지난 1월 개최된 ‘JP 모건 헬스케어 컨퍼런스’에서 ‘APX-311’의 기술 소개를 진행하고 글로벌 빅파마와 기술이전에 대한 심도 있는 미팅을 진행한 바 있다. 압타바
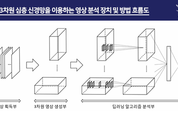
【 청년일보 】 제이엘케이는 ‘가상적 3차원 심층 신경망’(DNN, Deep Neural Network)을 이용하는 영상 분석 장치 및 방법’에 대한 미국 특허를 등록했다고 3일 밝혔다. 해당 기술은 MRI, CT와 같은 3차원 영상에서 축이 다른 복수의 2차원 영상데이터를 미리 설정된 순서대로 쌓아 가상 3차원 데이터로 재구축한, 뒤 각각의 방향으로 2차원 합성곱 신경망(CNN, Convolution Neural Network)을 적용해 3차원 CNN에 대비해 학습에 필요한 파라미터(Parameter)를 줄일 수 있는 알고리즘이다. 이러한 기술은 의료 분야와 같이 수집할 수 있는 데이터의 개수가 한정적인 인공지능 분야에서 특히 유효한 기술이다. 그만큼 국내외 인공지능 기반 의료 및 데이터 관련 분야에서 확장 가능성이 넓은 기술로 평가된다. 이번 특허로 글로벌 시장에서 제이엘케이의 한 단계 더 업그레이드된 R&D 기술력과 제품력에 대한 신뢰성을 재차 확보했다는 게 회사 측의 설명이다. 이번 발명은 제이엘케이의 의료 인공지능 플랫폼 ‘에이아이허브’(AIHuB) 및 토탈 데이터 매니지먼트 플랫폼 ‘헬로데이터’(Hello Data) 등 다양한 플랫폼의 3차

【 청년일보 】 T 세포 기반 면역 치료제 개발 기업 네오이뮨텍은 자사의 T 세포 증폭제 ‘NT-I7’을 활용한 진행성 다초점백질뇌병증 치료제 개발의 파일럿 임상에 대해 미국 식품의약국(FDA)으로부터 임상시험계획(IND) 승인을 획득했다고 3일 밝혔다. 진행성 다초점백질뇌병증(PML, Progressive Multifocal Leukoencephalopathy)은 평소 비활성 상태인 JC 바이러스(JCV, John Cunningham virus)가 활성화되면서 발생해 뇌의 염증 및 조직손상을 유발하는 질환이다. 주로 면역기능이 저하돼있는 후천면역결핍증후군(AIDS), 혈액암, 고형암, 류마티스 관절염, HIV 환자, 장기 면역 억제 치료를 받는 환자들에게서 발병하는 희귀질환으로 발병 후 수개월 내 치사율이 30~50%에 이르며 생존 환자에게도 심각한 신경계 장애가 나타나는 것으로 알려져 있다. 이번 IND 승인을 받은 임상은 ‘NT-I7’의 PML 치료제 개발을 위한 파일럿 연구(Pilot Study)에 대한 임상으로, 본임상 진입 전 해당 후보 물질의 실효성 및 적격성 등 검토하는 단계다. 네오이뮨텍은 PML 치료제로 연구 중인 ‘NT-I7’ 물질에 대해

【 청년일보 】 제이엘케이는 ‘뇌졸중 진단 및 예후 예측 방법 및 시스템’에 대한 미국 특허 등록에 성공했다고 2일 밝혔다. 이번 특허는 기존 국내 기술보증기금(KOREA TECHNOLOGY FINANCE CORPORATION)이 기술·사업성 평가에서 향후 7년 동안 매출 701억 원의 예상 가치를 인정했으며 이는 뇌졸중 관련 의료 인공지능 분야에서 독보적인 기술력을 의미한다. 제이엘케이는 이번 미국 특허 등록 성공 이후 국내를 넘어 세계적으로 한층 더 기술력 가치를 인정받는 계기가 될 것으로 보고있다. 뇌졸중은 뇌 영상과 의사의 숙련도에 크게 의존하는 병변이기 때문에 인공지능의 필요성이 대두되는 의료 분야 중 하나로 꼽힌다. 전 세계적으로 고령인구 증가로 인한 뇌졸중 환자 발생이 급격히 늘어나면서 사회·경제적 문제로 대두되고 있는데, 글로벌 의약품 시장조사기관 글로벌데이터(GlobalData)에 따르면 2025년 전 세계 뇌졸중 시장은 약 10조원을 넘을 것으로 전망하고 있다. 이번 미국 등록에 성공한 특허 기술은 뇌졸중을 정확하게 진단하고 뇌졸중의 환자 상태를 신뢰성 있게 예측할 수 있는 뇌졸중 진단 및 예후 예측 방법 및 시스템이다. 인간의 뇌 관련 복

【 청년일보 】 이중항체 전문기업 에이비엘바이오는 이중항체 면역항암제 ‘ABL111’의 임상 1상 계획(IND)을 미국 식품의약국(FDA)에 제출 완료했다고 2일 밝혔다. 중국 아이맵(I-Mab Biopharma)과 공동 개발 중인 ‘ABL111’은 위암과 췌장암을 포함한 여러 고형암에 발현하는 항원인 ‘클라우딘 18.2’(Claudin 18.2)와 면역세포를 활성화하는 ‘4-1BB’를 동시에 타깃하는 이중항체다. 인체의 면역력을 끌어올림으로써 암세포를 사멸하는 작용기전을 갖는다. ‘ABL111’은 동물실험에서 적은 용량으로도 암세포를 완전히 사멸시키는 높은 항암 효능을 입증했다. 종양에 재노출시켰을 때도 암을 기억하는 기억 T세포(memory T cell) 형성을 유도해 종양 성장을 억제하기도 했다. 반응률 역시 단독항체 면역항암제 또는 병용요법보다도 좋게 나타났다. 또한 ‘Grabody-T’ 플랫폼을 적용해 종양미세환경에서만 ‘4-1BB’가 활성화 되도록 해 기존 ‘4-1BB’ 항암제에서 흔히 나타나는 간독성 등의 부작용을 제거, 효과적이고 안전한 신약으로서의 가능성을 높게 평가받고 있다. 회사 관계자는 “‘ABL111’이 first-in-class 이중

【 청년일보 】 한미약품은 파트너사인 아테넥스가 미국 식품의약국(FDA)으로부터 전이성 유방암 치료를 위한 경구용 항암신약 ‘오락솔’의 시판허가에 대한 보완요구 서한(CRL, Complete Response Letter)을 받았다고 2일 밝혔다. 아테넥스에 따르면, FDA는 경구용 항암제인 오락솔이 정맥주사 대비 호중구 감소증 후유증 우려가 있다는 점을 제기했다. 아울러 FDA는 독립중앙심사위원회(BICR, blinded independent central review)가 19주차에 평가한 1차 평가 변수인 객관적반응률(ORR) 결과의 불확실성에 대한 우려를 표명했으며 추가적인 안전성 데이터 평가를 위해 미국 내 전이성 유방암 환자 대상의 적절한 신규 임상시험 수행이 필요하다고 조언했다. 잠재적 시판허가 승인을 위해 투여 용량 최적화 등 안전성을 개선할 수 있는 추가적 전략이 필요하다는 점도 알려왔다. 이에 아테넥스는 FDA 요구사항인 임상시험 설계 및 범위에 대해 논의하고 다음 단계로서 시판허가 승인 조율을 위한 미팅을 FDA에 요청할 계획이다. 아테넥스 측은 “이번 FDA의 결정을 매우 안타깝게 생각한다”면서 “오락솔의 시판승인을 얻기 위한 최선의 길을

【 청년일보 】 GC녹십자는 자사의 면역글로불린 제제인 ‘GC5107’(국내 제품명 아이비글로불린에스엔주 10%)에 대한 품목허가 신청서(BLA, Biologics License Application)를 미국 식품의약국(FDA)에 제출했다고 26일 밝혔다. 국내 혈액제제 중 글로벌 상업화를 앞둔 것은 이번이 처음이다. GC녹십자는 지난해 ‘GC5107’의 북미 임상 3상을 마무리했다. ‘일차 면역결핍증’(Primary Humoral Immunodeficiency) 환자를 대상으로 한 임상에서 FDA 가이드라인에 준한 유효성 및 안전성 평가 변수를 만족시켰다. 유효성 측면에서 ‘GC5107’을 투약해 12개월 간 ‘급성 및 중증 세균성 감염’(Acute Serious Bacterial Infections) 빈도를 측정한 결과, FDA 기준인 1보다 낮은 0.02의 수치를 나타냈다. 안전성 평가에서도 약물로 인한 사망이나 심각한 수준의 이상반응이 관찰되지 않는 등 모든 기준을 충족시키는 결과를 보였다. 미국 면역글로불린 시장은 약 81억 달러 규모를 형성하고 있으며, 최근 자가면역질환의 증가로 면역글로불린에 대한 수요는 지속적으로 증가하는 추세다. 하지만 대규모

【 청년일보 】 차바이오텍은 미국 자회사 ‘마티카 바이오테크놀로지’가 세포유전자 치료제 위탁개발생산(CDMO) 사업을 위한 생산시설 기공식을 텍사스주 칼리지스테이션시 부지에서 열었다고 24일 밝혔다. 이 시설은 미국 식품의약국(FDA)이 인정하는 의약품 제조 및 품질관리기준 인증(cGMP)을 받았다. 마티카바이오는 이곳에 500ℓ 용량의 바이오리액터와 제조설비를 구축, 차세대 항암제 등 세포 유전자 치료제에 활용될 바이럴벡터를 생산할 예정이다. 마티카바이오는 지난해 12월 칼리지스테이션 시 텍사스 A&M 대학교 캠퍼스에 공장 부지 리스 계약을 하고 공장 설계에 착수했다. 올해 말 완공 예정이며 이 시설에서 미국 현지 고객사를 대상으로 바이럴벡터의 개발, 제조 등의 서비스를 제공할 계획이다. 차바이오텍 오상훈 대표는 “마티카바이오는 차바이오텍의 글로벌 세포유전자치료제 사업의 교두보 역할을 할 것”이라며 “오는 2024년 완공될 제2판교테크노밸리 GMP 시설과 연계해 글로벌 CDMO 시장에서 경쟁력을 확보하겠다”고 말했다. 【 청년일보=안상준 기자 】

【 청년일보 】 메디톡스와 대웅제약의 ‘보툴리늄 톡신 전쟁’이 마무리 국면에 접어들었다. 메디톡스 측이 에볼루스로부터 합의금과 로열티 등을 받는 조건으로 대웅제약의 보툴리눔 톡신 제제 ‘나보타’(미국 제품명 주보)의 미국 판매를 허용하기로 결정하면서다. 다만, 양사간 미국 시장에서의 전면전이 ‘일단락(?)된 분위기와 달리 양사간 진행 중인 국내 소송은 예정대로 추진하겠다는 입장이어서 여전히 분쟁의 불씨가 남아 있는 상황이란 분석이 나온다. 23일 제약·바이오업계 등에 따르면, 메디톡스는 최근 엘러간·에볼루스 등과 ‘3자간 합의’ 계약을 체결했다. 이에 따라 미국 국제무역위원회(ITC)의 ‘나보타’ 판매금지 결정은 물론, 메디톡스가 에볼루스를 상대로 제기한 미국 캘리포니아 소송 등도 모두 철회될 예정이다. 엘러간은 한국을 제외한 전 세계 국가에서 메디톡스의 보툴리눔 톡신 신 제제(MT10109L) 독점 판매권을 보유하고 있으며, 에볼루스는 한국을 제외한 전 세계의 ‘나보타’ 독점 판매권을 쥐고 있는 대웅제약의 파트너사다. ◆ 메디톡스·엘러간·에볼루스 3자 합의…핵심은 "합의금과 로열티" 메디톡스·엘러간·에볼루스 이들 3자간 합의의 핵심은 메디톡스와 엘러간이 에

【 청년일보 】 메디톡스는 대웅제약의 미국 파트너사 에볼루스(EVOLUS) 주식 16.7%를 취득해 2대 주주가 된다고 22일 밝혔다. 이번 주식 취득은 미국 국제무역위원회(ITC)의 대웅제약 보툴리눔 톡신 제제 ‘나보타’(수출명 주보) 수입금지 21개월 결정을 두고 메디톡스·엘러간·에볼루스 3자간 합의한 데 따른 것이다. 대웅제약은 이번 합의 당사자가 아니다. 이에 따라 메디톡스는 에볼루스 보통주 676만2,652주를 약 535억원에 취득했다. 에볼루스는 주당 0.0001달러로 보통주를 신규 발행했다. 이번 합의로 대웅제약과 메디톡스는 ITC 위원회에 소송이 제기되기 전의 상태로 돌아갔고 대웅제약은 미국 내 나보타 사업을 재개할 수 있게 됐다. 에볼루스가 보유한 미국 내 재고도 판매할 수 있다. 에볼루스는 메디톡스와 엘러간에 합의금 총 3,500만달러(한화 약 380억원)를 2년간 분할해 지급하고 나보타 매출에 따른 로열티를 지급하기로 했다. 【 청년일보=안상준 기자 】

【 청년일보 】 대웅제약은 미국 연방순회항소법원(US Court of Appeals for the Federal Circuit, CAFC)에 신청한 수입금지 명령 집행정지 관련 긴급 임시가처분 신청(emergency motion to interim stay)이 인용됐다고 16일 밝혔다. 이는 지난 12일 가처분을 신청한 지 3일 만에 신속히 인용된 것으로, 이에 따라 지난해 12월 미국 국제무역위원회(ITC)가 21개월 수입금지 명령을 내린 보툴리눔 톡신 제제 ‘나보타’(미국 수출명 주보)의 판매가 공백 없이 재개될 수 있게 됐다. 공탁금(bond) 조건은 종전과 동일하며, 미국 국제무역위원회(ITC) 공탁금과 마찬가지로 이 공탁금 또한 항소심 또는 대법원의 최종 판결에 따라 수취인이 결정된다. 즉, 에볼루스가 항소심 또는 대법원 최종판결에서 승소하게 되면 공탁금 전액을 돌려받게 된다. 긴급 가처분은 항소법원의 본 가처분 인용 결정 시까지 유효하며 대웅제약을 대리하는 로펌 Goldstein and Russell은 주보의 원활한 판매를 위해 공탁금 없이 인용될 수 있도록 지난 12일(미국 현지시간) 가처분 신청을 완료했다. 한국과 달리 미국 항소법원은 가처분을

【 청년일보 】 네오이뮨텍은 자사의 ‘NT-I7’(efineptakin alfa)과 글로벌 제약 기업 BMS의 면역관문억제제 ‘옵디보’(Opdivo)와의 병용 투여에 대해 미국 현지에서 임상 2상을 진행 중이며, 최근 첫 투약을 시행했다고 16일 밝혔다. 회사 측은 전이성 위암, 위·식도 접합부 암, 식도선암 등의 타깃 암종에 대해 미국 식품의약국(FDA)으로부터 임상시험계획(IND) 승인을 획득한 뒤 임상환자 모집을 시작했다. 이번 임상은 T세포 증폭을 유도하는 ‘NT-I7’과 PD-1 차단 항체 ‘옵디보’ 병용투여 환자 그룹과 ‘옵디보’ 단독투여 환자그룹 간의 비교를 통해 안전성 및 항암 효능을 평가할 예정이다. ‘NT-I7’은 네오이뮨텍이 개발 중인 T세포의 증폭을 유도하는 퍼스트 인 클래스 차세대 면역 항암제로, 단독 요법의 효능뿐 아니라 기존 항암치료제와 병용 투여 시 치료 효과의 시너지가 기대되는 신약이다. 네오이뮨텍 양세환 대표이사는 “안전성이 입증된 ‘NT-I7’을 ‘옵디보’와 같은 면역관문억제제와 병용하면 T세포 증폭, T세포 활성화 등의 시너지를 통해 항암효과를 극대화할 수 있을 것으로 기대된다”며 “특히 1차, 2차 치료 후 재발된 위암