
【 청년일보 】 엔케이맥스는 식약처로부터 슈퍼NK(SNK01), GC(Gemcitabine Carboplatin), 얼비툭스 3종을 병용투여하는 국내 임상 1/2a상을 승인받았다고 7일 밝혔다. 이로써 엔케이맥스가 추진 중인 임상은 한국 2개, 미국3개, 멕시코 2개 등 총 7개가 됐다. 엔케이맥스가 이번에 추가한 임상은 TKI(Tyrosine kinase inhibitor, 티로신키나아제 저해제) 치료에 실패한 비소세포폐암 환자를 대상으로 하며 서울 소재 한 병원에서 진행할 계획이다. TKI 치료에 실패할 경우 현재 적합한 치료요법이 없는 상황이다. TKI는 대표적인 비소세포폐암 1차 치료제로, 암세포의 성장을 유도하는 티로신키나아제(Tyrosine kinases) 단백질의 기능을 억제하는 약물이다. 본 임상은 총 24명의 환자들을 대상으로 진행되며, 우선 4개의 코호트로 환자를 분류해 슈퍼NK와 GC 및 얼비툭스를 병용 투여한다. 코호트1 및 코호트3의 환자군 12명에게는 슈퍼NK(40억개 및 60억개)와 GC를 병용투여하며 코호트2 및 코호트4의 환자군 12명에게는 슈퍼NK(40억개 및 60억개)와 GC, 얼비툭스 3가지 약물을 병용 투여한다. 이후 용
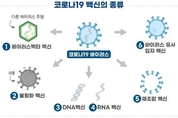
【 청년일보 】 식품의약품안전처는 SK바이오사이언스가 개발 중인 코로나19 백신 ‘GBP510’에 대한 임상 1/2상 시험을 승인했다고 31일 밝혔다. 이번 임상은 건강한 성인을 대상으로 ‘GBP510’의 안전성 및 면역원성을 평가하기 위한 것으로, 1상 진행 후 2상을 순차적으로 진행하게 된다. ‘GBP510’은 코로나19 바이러스의 ‘표면항원 단백질’을 유전자 재조합 기술을 이용해 만든 ‘재조합 백신’이다. 예방원리는 백신의 표면항원 단백질이 면역세포를 자극해 중화항체를 형성, 면역반응을 유도하며 코로나19 바이러스가 침입하는 경우 항체가 코로나19 바이러스를 제거하게 된다. SK바이오사이언스가 지난 11월 23일 임상 1상을 승인받은 재조합백신 ‘NBP2001’는 코로나19 바이러스의 표면 항원 단백질로 면역반응을 유도하며 ‘GBP510’는 표면 항원 단백질이 나노구조(정20면체)를 형성하는 특정 단백질과 결합해 면역반응을 유도하는 차이가 있다. 해외에서도 미국 노바백스가 유전자 재조합 기술을 이용한 코로나19 백신의 임상 3상을 진행하고 있다. 식약처는 관계자는 “앞으로도 코로나19 치료제·백신 개발에 대한 국민적 관심이 높은 점 등을 고려해 개발 제

【 청년일보 】 GC녹십자랩셀은 미국 현지법인 아티바 바이오테라퓨틱스가 미국 식품의약국(FDA)으로부터 자연살해(NK, Natural Killer) 세포치료제 ‘AB101’의 임상 1·2상 시험계획을 승인받았다고 8일 밝혔다. 이번 임상에서는 기존 치료제를 투여한 재발 및 불응성 림프종 환자를 대상으로 안전성과 유효성을 평가한다. 미국 내 총 20개 암센터에서 진행된다. ‘AB101’은 림프종 치료를 목적으로 항체치료제를 병용하는 제대혈 유래 방식의 차세대 NK세포치료제다. 앞선 동물실험에서 생존율 및 종양 억제 능력 등 항암효과가 기존 치료제보다 개선된 것으로 확인됐다는 게 회사 측의 설명이다. 아티바는 지난해 녹십자홀딩스(GC)와 GC녹십자랩셀이 미국 샌디에이고에 설립한 법인으로 ‘AB101’을 기반으로 하는 양산 기술과 GC녹십자랩셀의 NK세포치료제 파이프라인 기술을 도입해 상업화를 추진하고 있다. 이번 임상은 GC녹십자랩셀과 아티바의 첫 협업 과제다. 아티바는 ‘AB101’을 시작으로 GC녹십자랩셀 기술 기반 ‘AB200’ 시리즈의 미국 임상을 내년부터 진행할 계획이다. 이를 위해 아티바는 올해 6월 투자금 7,800만 달러(한화 약 846억원)를 유

【 청년일보 】 JW중외제약은 중국 의약품관리국(NMPA)으로부터 통풍 치료제로 개발 중인 ‘URC102’의 임상 1상 시험 계획을 승인 받았다고 2일 밝혔다. ‘URC102’는 지난해 JW중외제약이 중국 심시어 파마슈티컬에 기술 수출한 물질이다. 심시어는 올해 8월 중국 NMPA에 ‘URC102’(심시어 프로젝트명 SIM1909-13)의 임상 시험 계획서를 제출한 바 있다. 심시어는 이번 임상 시험계획 승인에 따라 상하이 공중 보건 임상 센터(Shanghai Public Health Clinical Center)에서 총 40명의 건강한 중국인을 대상으로 안전성, 내약성 등을 평가할 예정이다. JW중외제약은 총 140명의 한국인 통풍 환자들을 대상으로 진행한 ‘URC102’의 임상 2a상에서 높은 안전성과 혈중 요산수치 감소효과를 입증한 바 있다. 이어 진행한 임상 2b상은 지난달 피험자 투약을 완료하고 현재 임상 데이터를 수집하고 있다. 임상 2b상의 결과보고서는 2021년 초에 도출될 예정이다. JW중외제약 이성열 대표는 “이번 중국 임상계획 승인으로 ‘URC102’의 해외 첫 임상을 시작하게 됐다”며 “‘URC102’의 개발이 신속히 마무리 돼 통풍으로